食藥署今(7日)公布了一則重要藥品回收通知,涉及由信東生技股份有限公司生產的前列腺肥大症藥品。據報導,該公司的「信東護列淨持續釋放膠囊0.2毫克」在其18個月的安定性測試中,發現其溶解度已趨近於規格下限的13%,可能會導致藥效受影響。因此,該公司已主動向食藥署通報,並開始回收該產品。
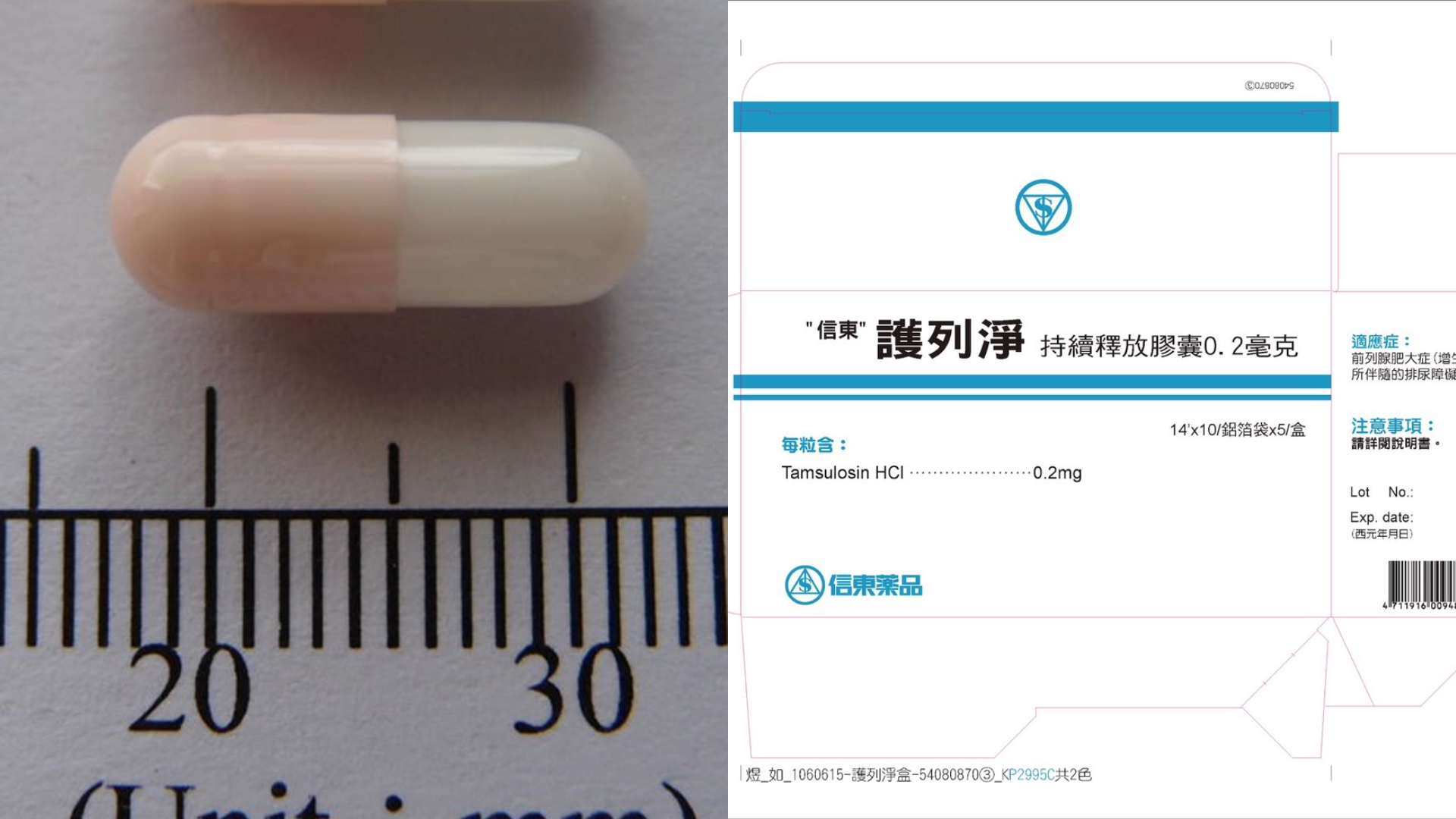
▲信東護列淨持續釋放膠囊0.2毫克藥效恐受影響,食藥署預防性回收170萬顆。(圖/食藥署提供)
食藥署副署長陳惠芳說明,根據國際藥品檢驗合作組織(PIC/S)的規定,藥品在達到其效期之前,每半年都需要進行一次安定性測試以確保其品質。信東生技所生產的這款藥品主要用於治療前列腺肥大症所引起的排尿障礙,其效期為2年。
受影響的批次包括7BP1059、7TD1083、7TD1084、7TN1791、7BK1071、7BP1060、7TD1082、7TN2552、7BP1061、7BK1070、7TN2551、7BK1069,共12個批號,總計需要回收170萬顆藥品。

▲信東護列淨持續釋放膠囊0.2毫克藥效恐受影響,食藥署預防性回收170萬顆。(圖/食藥署提供)
儘管這款藥品在過去一年中的健保用量為110萬顆,市場佔有率並不高,而且市場上還有5種同樣成分的學名藥可供替換,所以此次的回收行動不會對公眾的用藥需求造成影響。食藥署已要求信東生技於今年8月24日前完成回收工作,並需要提交回收報告以及後續的預防矯正措施。
食藥署也提醒,如果民眾對正在使用的藥品有任何疑問或擔憂,應儘快與醫生討論,並由醫生處方其他適當的藥品。食藥署呼籲醫療院所、藥商、和藥局配合進行回收工作,並立即停止調劑和供應相關藥品。













留言評論